Un equipo del Centro Nacional de Investigaciones Cardiovasculares (CNIC), liderado por el Profesor Miguel Ángel del Pozo Barriuso, jefe de grupo de Mecanoadaptación y Biología de Caveolas del CNIC, ha identificado un mecanismo esencial en las células grasas (adipocitos) que les permite expandirse de manera segura para almacenar energía. Este proceso evita daños en los tejidos y protege al organismo de las consecuencias tóxicas de la acumulación de lípidos en lugares inadecuados. Los resultados, publicados en la revista ‘Nature Communications’, suponen un avance significativo en la comprensión de las enfermedades metabólicas. Además, este descubrimiento abre la puerta al desarrollo de nuevas estrategias terapéuticas para combatir las enfermedades relacionadas con exceso energético crónico, como el sobrepeso, la obesidad, la lipodistrofia y el síndrome metabólico, y sus graves complicaciones cardiovasculares y metabólicas.

En una sociedad caracterizada por el sedentarismo y dietas ricas en calorías, el tejido adiposo juega un papel crucial en la salud metabólica. Los adipocitos tienen la capacidad de expandirse enormemente para almacenar energía en forma de grasa, previniendo que el exceso lipídico se acumule en órganos como el hígado o las paredes de los vasos sanguíneos (especialmente los del corazón y cerebro), donde podría causar daños irreversibles.
Sin embargo, este proceso no está exento de riesgos: una sobrecarga de grasa puede provocar la ruptura de los adipocitos, liberando su contenido tóxico y generando inflamación y alteraciones metabólicas.
El estudio del CNIC se centra en cómo los adipocitos se adaptan para soportar las tensiones mecánicas derivadas de su expansión para acomodarse a la grasa acumulada.
El equipo analizó el papel de las caveolas, unas pequeñas invaginaciones en la membrana celular que actúan como sensores y amortiguadores de estas tensiones. “Cuando el adipocito acumula grasa y su superficie se somete a mayor tensión, las caveolas se aplanan, liberando un “reservorio” de membrana que permite que la célula se expanda sin romperse. Por contra, cuando las reservas de grasa disminuyen, estas estructuras se reagrupan para reducir el exceso de membrana y restaurar la estabilidad celular”, explica la Dra. María Aboy Pardal, primera autora de la investigación.
Caveolas: más que un soporte estructural
Además de proteger físicamente a los adipocitos, las caveolas cumplen un rol esencial en la coordinación del metabolismo celular. Durante el proceso de expansión, detalla el Dr. Miguel Ángel del Pozo Barriuso, “componentes moleculares de estas estructuras viajan hacia otros compartimentos de la célula, enviando señales que ajustan la actividad metabólica al nivel de reservas energéticas. Esta capacidad de ‘comunicarse’ internamente convierte a las caveolas en elementos clave para el funcionamiento eficiente del adipocito”.
Sin embargo, cuando estas estructuras faltan o no funcionan correctamente, los adipocitos se vuelven más rígidos, vulnerables a rupturas y menos eficientes en la acumulación de energía. Como resultado, añade la Dra. Aboy Pardal, “se genera inflamación y se compromete la salud metabólica del organismo. Este fenómeno está relacionado con enfermedades como la lipodistrofia, una condición en la que los pacientes son incapaces de formar depósitos grasos, lo que deriva en alteraciones metabólicas y cardiovasculares graves”.
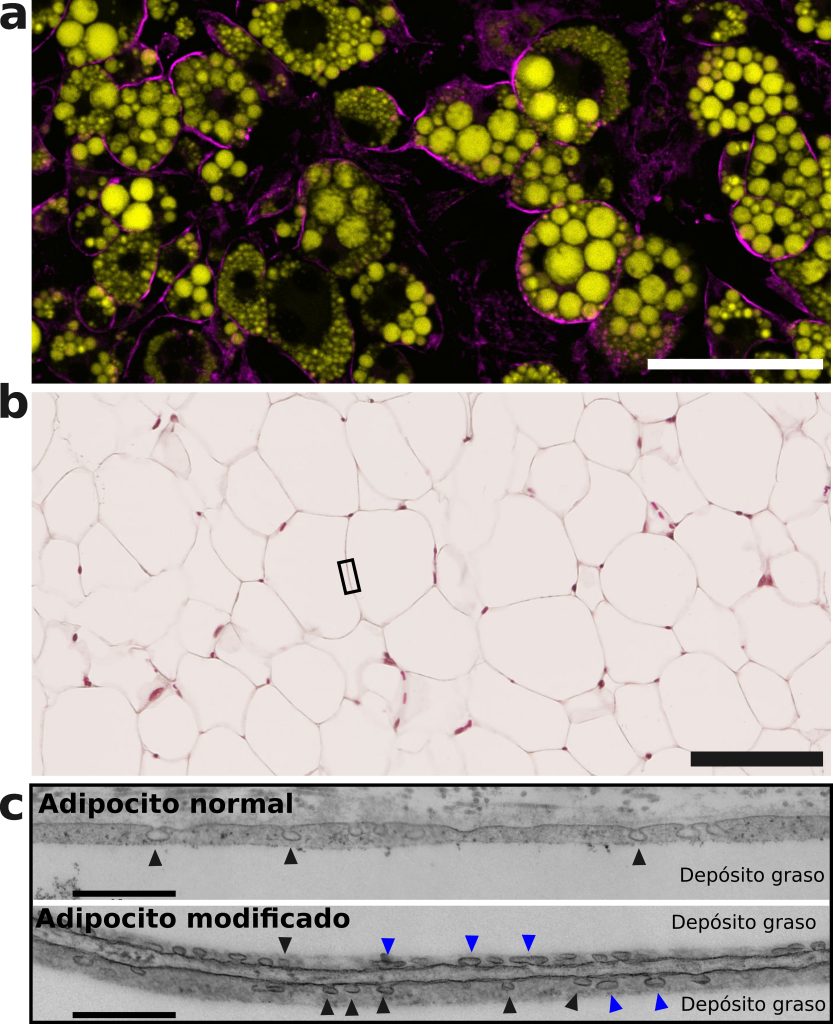
Asimismo, el estudio del CNIC destaca el papel de una proteína clave, Caveolina-1 (Cav1), en el proceso de reorganización de las caveolas. Esta proteína necesita ser fosforilada (modificada químicamente) en un aminoácido específico para permitir que las caveolas se aplanen adecuadamente en respuesta a las fluctuaciones de tensión mecánica en la membrana celular. Los investigadores desarrollaron un ratón transgénico que expresaba una forma modificada de Cav1 que es incapaz de fosforilarse. En dicho ratón, es decir cuando la fosforilación de Cav1 no se produce, los adipocitos no pueden expandirse correctamente ante la tensión ejercida por la acumulación de grasa (ver imagen), lo que impacta negativamente en su capacidad de almacenar energía y mantener la integridad de la célula. El fallo de este mecanismo tan básico conduce finalmente a la lipodistrofia y sus graves consecuencias.
El Profesor Miguel Ángel del Pozo concluye que “estos resultados nos permiten entender mejor cómo el tejido adiposo responde a las fuerzas mecánicas asociadas con el exceso energético. En un contexto de obesidad y síndrome metabólico, este mecanismo de protección es clave para minimizar los daños en el organismo”.
La investigación ha contado con la colaboración de las Unidades de Transgénesis, Tecnología de Células Pluripotentes, Microscopía e Histopatología del CNIC. Además, han colaborado investigadores del Instituto de Ciencia de Materiales de Madrid (ICMM, CSIC); Centro de Investigación en Medicina Molecular y Enfermedades Crónicas CIMUS; CNIO; Instituto de Investigaciones Biomédicas ‘Sols-Morreale’; y Centro de Investigaciones Biológicas Margarita Salas –CSIC.

