Un equipo del Instituto de Microelectrónica de Barcelona (IMB-CNM) del CSIC, organismo adscrito al Ministerio de Ciencia, Innovación y Universidades, y la Universidad Autónoma de Barcelona ha diseñado un microdispositivo pionero que convierte el movimiento del propio tejido en impulsos eléctricos capaces de estimular células de forma localizada. Su tamaño, comparable al de una célula, permite actuar sobre regiones muy concretas del organismo sin necesidad de cables, baterías, ni cirugía profunda. El dispositivo, aún en fase experimental, se ha probado en cultivos celulares, donde ha demostrado su capacidad para inducir respuestas eléctricas localizadas. Este avance abre nuevas posibilidades para terapias inalámbricas de estimulación controlada de células mediante impulsos eléctricos (electromodulación), con aplicaciones potenciales en el futuro en enfermedades degenerativas, neurológicas o musculares, así como en procesos de regeneración y cicatrización. El trabajo se ha publicado en la revista Advanced Science.
Este microdispositivo se encuadra en una nueva generación de tecnologías médicas que utilizan la estimulación eléctrica en lugar de fármacos para modular funciones biológicas (electroceuticals). A diferencia de dispositivos convencionales como los marcapasos, que actúan sobre grandes zonas del cuerpo, estos microdispositivos permiten una medicina más precisa y personalizada, con menos efectos secundarios.
Versatilidad
El dispositivo está formado por diminutas partículas de silicio, similares en tamaño a una célula, que están recubiertas con una capa de óxido de zinc. Este material tiene una propiedad especial llamada piezoelectricidad, que permite generar pequeños campos eléctricos cuando se deforma, por ejemplo, bajo presión o movimiento. Esta propiedad permite que el dispositivo se active con los propios movimientos de las células del tejido donde se encuentra, sin necesidad de fuentes externas de energía.
“El proceso de fabricación del microdispositivo ofrece una gran versatilidad, ya que permite ajustar tanto el tamaño de las partículas de silicio como las dimensiones de las nanoláminas, facilitando su adaptación a los distintos requerimientos de estimulación de cada tipo celular”, explica Laura Lefaix, investigadora predoctoral en el IMB-CNM y primera autora del estudio.
La investigación ha demostrado que el dispositivo puede generar un campo eléctrico suficiente para inducir respuestas celulares, como el aumento de calcio intracelular, que es un indicador de activación. Para ello, se optimizó el grosor y la forma de nanoláminas de óxido de zinc (láminas con un grosor de millonésimas de milímetro), de modo que fueran lo bastante sensibles al movimiento celular pero también estables estructuralmente.
“Al ajustar el diseño de las nanoestructuras que forman parte del dispositivo, conseguimos que respondan mejor al movimiento de las células y generen electricidad de forma más eficiente. Además, al modificar el tamaño de la base del dispositivo, podemos controlar con mayor precisión dónde se coloca y cómo interactúa con cada célula individual”, señala Lefaix.
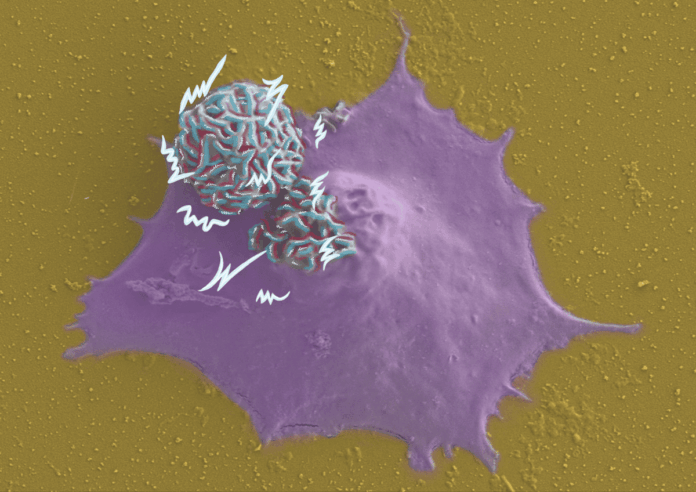
Además de su capacidad para estimular células, el estudio ha abordado un aspecto clave para su aplicación terapéutica, como la internalización celular. Cuando un dispositivo es demasiado pequeño, puede ser absorbido por las células, lo que dificulta controlar su efecto y puede alterar procesos internos. En este trabajo, se probaron tres tamaños distintos de micropartículas en dos tipos de células del hueso: osteoblastos sanos y células tumorales de osteosarcoma.
Los resultados muestran que las células tumorales llegaron a absorber hasta un 50 % de los dispositivos más pequeños, mientras que en las células sanas la absorción fue inferior al 10 %. Esta diferencia se debe a que las células tumorales tienen mecanismos de absorción más activos, como la macropinocitosis, que les permite incorporar partículas de mayor tamaño. En cambio, las células sanas tienden a mantener los dispositivos en el exterior, en contacto con la membrana celular, lo que permite una estimulación más controlada y segura. Este control sobre la localización del dispositivo para que permanezca fuera de la célula es esencial para garantizar que el campo eléctrico actúe sobre la membrana celular, que regula funciones generales (proliferación o diferenciación celular) y específicas de cada tejido (contracción muscular o transmisión del impulso nervioso).
Terapias inalámbricas a nivel celular
La capacidad de actuar desde el exterior de la célula, junto con su diseño basado en tecnología de silicio, convierte a estos microdispositivos en una futura herramienta muy prometedora. “Estos microdispositivos abren el camino a terapias inalámbricas a nivel celular, mucho más precisas y seguras. A diferencia de las nanopartículas, permiten controlar mejor el estímulo en cada célula y, gracias a estar basados en tecnología de silicio, tienen un enorme potencial para aplicaciones biomédicas avanzadas”, destaca Gonzalo Murillo, coordinador del proyecto y Premio Nacional de Investigación para Jóvenes “Ángela Ruiz Robles” 2023.
El diseño del dispositivo se basa en materiales biocompatibles, como el óxido de zinc, que pueden interactuar con tejidos vivos sin provocar efectos tóxicos, inflamatorios ni inmunológicos adversos. Además, su compatibilidad con tecnologías MEMS (sistemas microelectromecánicos) permite incorporar sensores, actuadores o circuitos de control en plataformas miniaturizadas. Esta versatilidad abre la puerta a dotar a este dispositivo en desarrollo de funcionalidades adicionales, como la capacidad de responder a estímulos externos, como ultrasonidos, o registrar información sobre el entorno celular.
La fabricación se ha realizado íntegramente en la Sala Blanca de Micro y Nanofabricación del IMB-CNM, aprovechando la experiencia del instituto en el desarrollo de micropartículas para aplicaciones biomédicas. El proceso permite producir dispositivos de forma escalable y personalizada, adaptándolos a distintos tipos celulares y necesidades terapéuticas.
Este trabajo representa un paso importante hacia el desarrollo de terapias eléctricas de alta precisión, capaces de actuar a nivel celular sin invadir el interior de las células ni requerir intervenciones complejas. Su potencial para modular funciones biológicas de forma localizada y autónoma lo convierte en una herramienta prometedora para la medicina del futuro.